近日,《Small Methods》(IF:14.188)发表了暨南大学生物医学工程学科研究团队戴箭副研究员与薛巍研究员关于筛选最优尺寸人造纳米“血小板”实现肿瘤血管处精准启动凝血的最新重要发现:“Artificial Nanoplatelets Depend on Size for Precisely Inducing Thrombosis in Tumor Vessels”。

1. 文章概述
戴箭副研究员与薛巍研究员团队开发了一种能够用于肿瘤血管处精准启动凝血的人造纳米“血小板”——肿瘤血管栓塞剂,将凝血酶高效、特异地递送到肿瘤血管部位,以实现肿瘤组织快速、大面积的坏死。同时,为了更好地设计出高效的肿瘤血管栓塞剂,本项目创新性地探索了不同尺寸的人造纳米“血小板”(200 nm、400 nm 和 800 nm)对肿瘤血管堵塞的效果的影响,以筛选出最优尺寸的肿瘤血管栓塞剂。
2. 图文导读
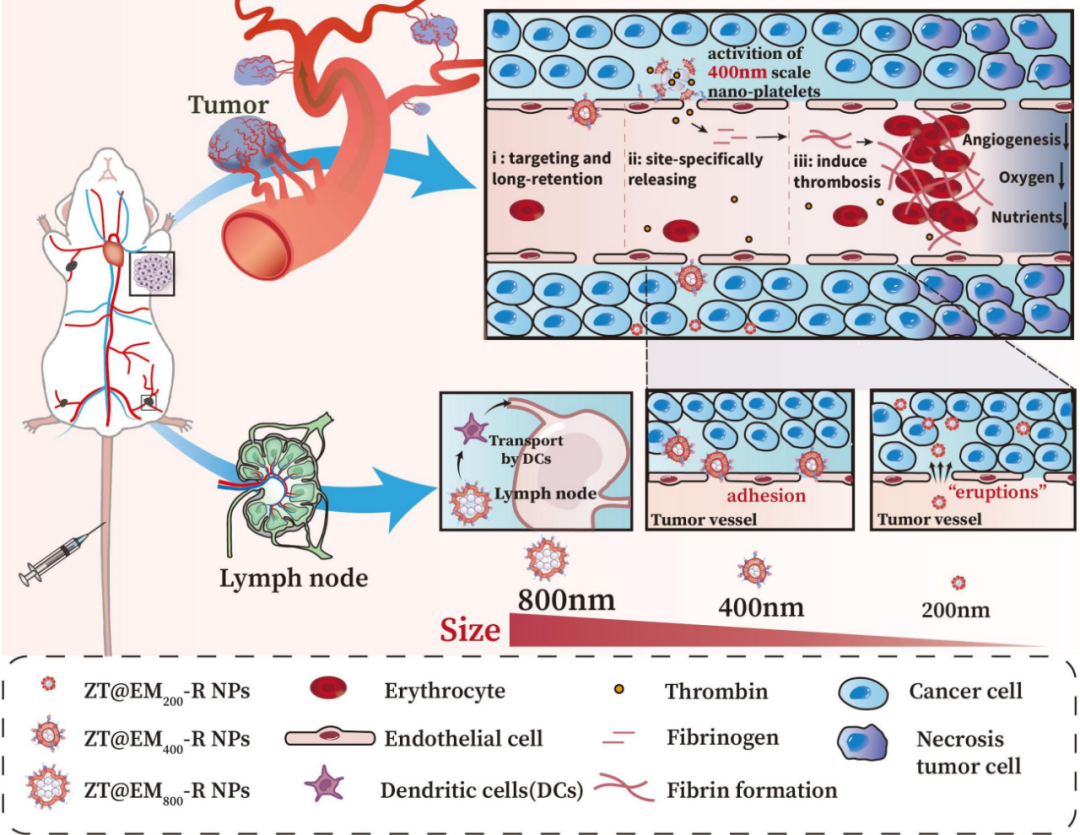
【图1】 肿瘤血管处精准启动凝血的人造纳米“血小板”的抗肿瘤机制及其尺寸效应
如图1,人造“血小板”的大小会影响其生物分布(如图中三个小框),400 nm的人造“血小板”能够有效地停留在肿瘤血管附近,释放凝血酶以诱导血栓形成。相比之下,200 nm的人造“血小板”倾向于从肿瘤血管渗出到肿瘤组织深处,而800 nm的人造“血小板”则明显累积到淋巴结。其中,与其他两个尺寸组相比,400 nm尺寸是人工纳米血小板精确堵塞肿瘤血管的最适尺寸。肿瘤血管处精准启动凝血的人造纳米“血小板”的抗肿瘤机制如下:i)首先人造纳米“血小板”由于cRGD靶向肽以及400 nm合适的尺寸效应,可以紧紧粘附在肿瘤血管内皮并在血管处累积;ii)人造纳米“血小板”累积到肿瘤血管处并特异性释放凝血酶;iii)人造“血小板”诱导内源性的凝血,从而切断肿瘤的营养和氧气供应,导致肿瘤的消融。
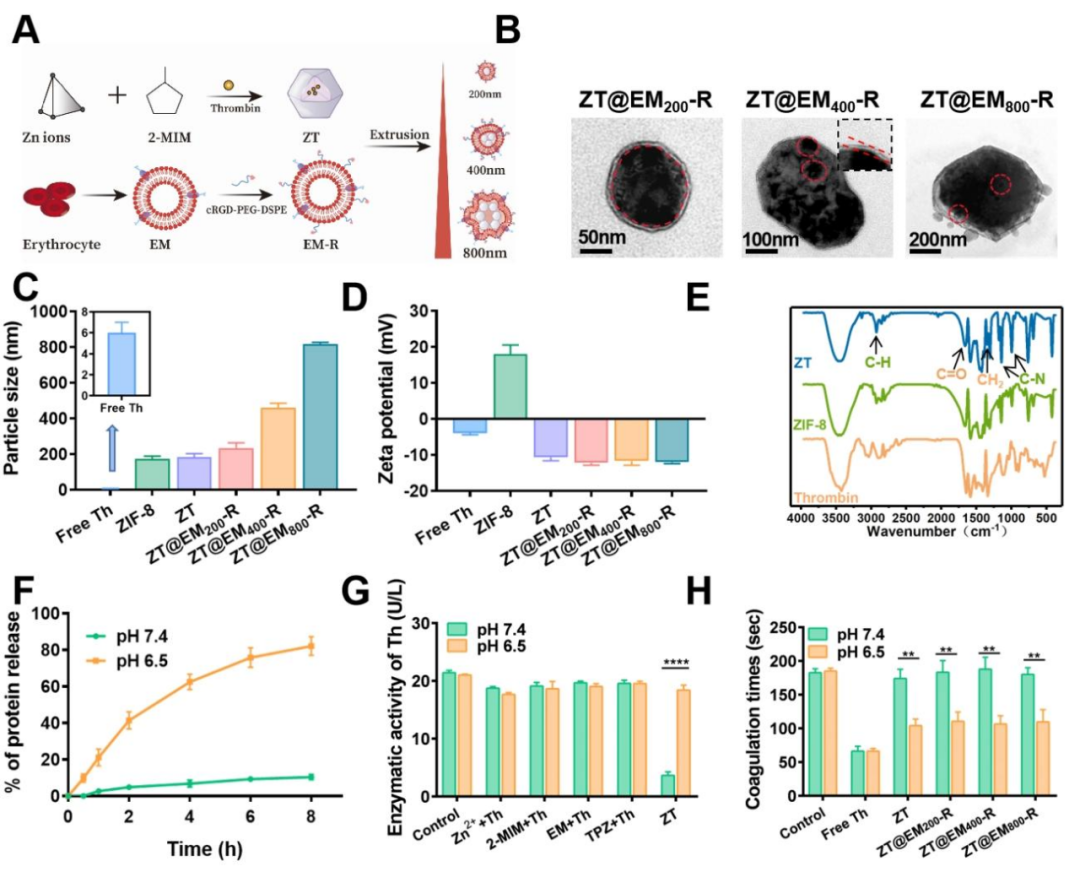
【图2】人造纳米“血小板”的合成与表征。
如图2,人造纳米“血小板”(ZT@EM-R)的制备分为两步,首先通过沸石咪唑骨架-8(ZIF-8)负载凝血酶(Thrombin),得到ZT纳米粒子;接着通过共挤出的方式制备带有靶向肽的红细胞膜包覆ZT纳米粒子,也就是人造纳米“血小板”。通过挤出不同大小的聚碳酸酯多孔膜分别制备出不同尺寸(200、400、800 nm)的人造纳米“血小板”(ZT@EM200-R,ZT@EM400-R和ZT@EM800-R)。同时,利用ZIF-8可响应肿瘤微酸环境释放凝血酶,可实现人造纳米“血小板”在肿瘤部位的精准激活,进一步启动凝血。
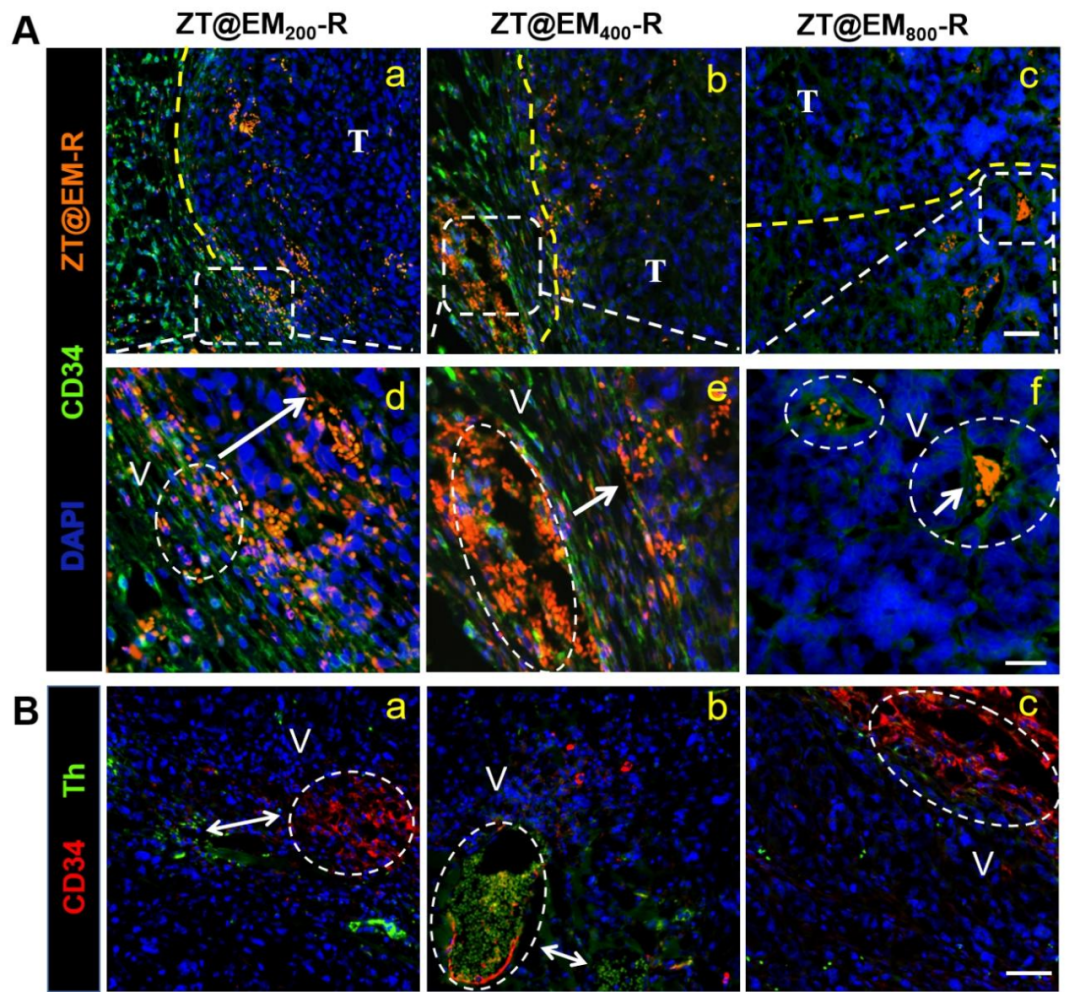
【图3】人造纳米“血小板”和凝血酶的肿瘤血管分布情况。
考虑到药物的分布可直接影响其治疗效果,我们还探究了不同尺寸的人造纳米“血小板”在肿瘤部位的分布情况。如图3,200 nm尺寸的人造“血小板”主要分布在肿瘤组织处并且远离血管部位,这表明200 nm尺寸的人造“血小板”可能渗透出肿瘤血管,被“冲到”肿瘤组织的深处。由于释放后的凝血酶远离血管,因此难以回到血管部位启动凝血;此外,800 nm尺寸的人造“血小板”在肿瘤血管部位积累较少,结合活体成像结果表明这可能是大尺寸的纳米粒子易被免疫细胞吞噬并随之累积到淋巴结部位。相比而言,400 nm尺寸的人造“血小板”大部分集中在血管部位或者稍微穿过血管,因此释放的凝血酶可以大量集中在肿瘤血管部位。说明400 nm是用于制备肿瘤血管精准启动凝血人造纳米“血小板”的最佳尺寸。
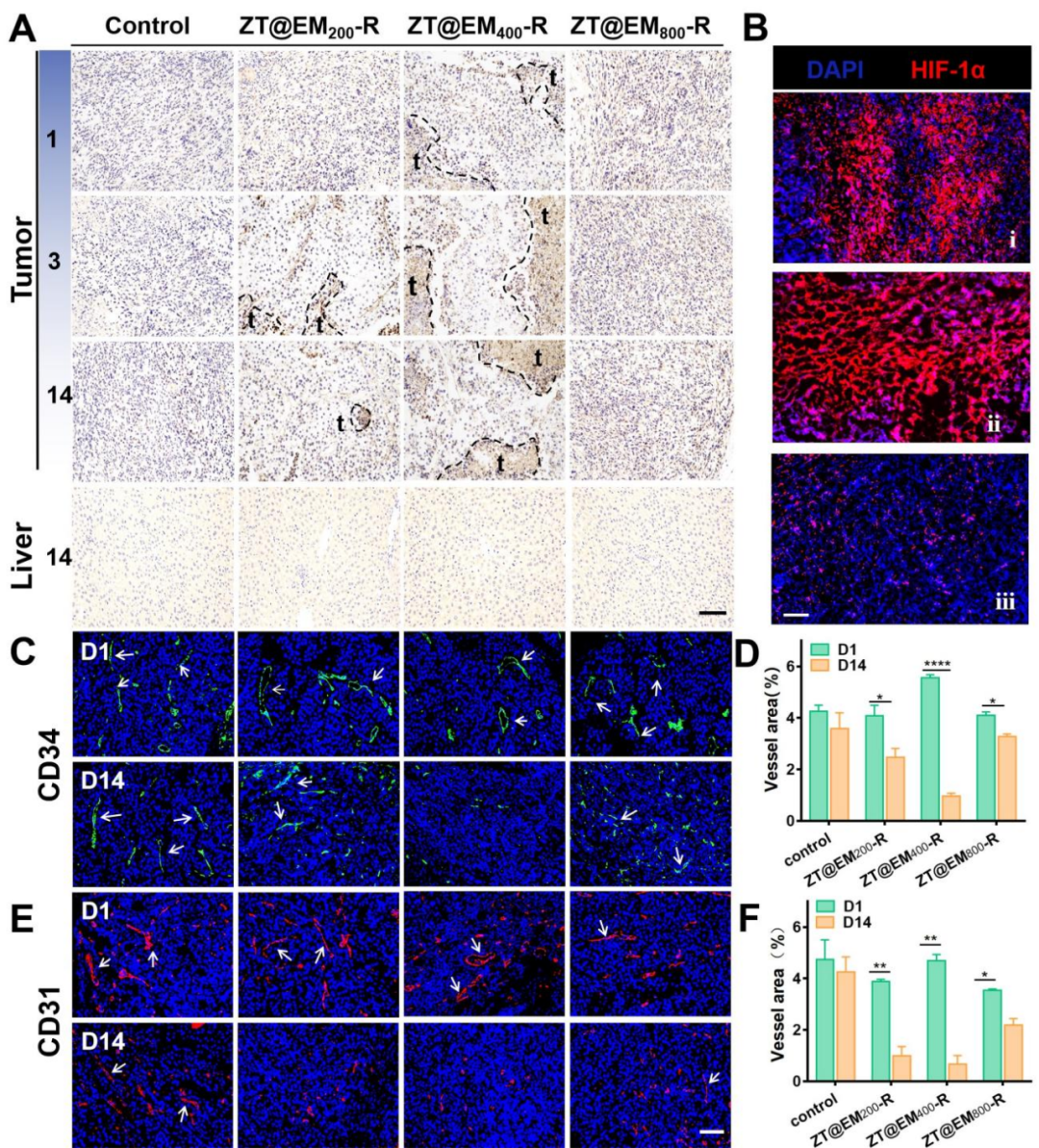
【图4】在肿瘤血管系统中通过人造纳米血小板诱导血栓形成。
释放的凝血酶可将血液中的纤维蛋白原转化为纤维蛋白,促进形成稳定的血栓。为了验证血栓在肿瘤血管部位的形成,我们通过CD41免疫染色来检验肿瘤部位是否存在活化血小板的聚集。如图4所示,400 nm尺寸的人造“血小板”组别中可以明显看到肿瘤区域有致密血栓形成并且在整个治疗期间持续存在。同时各组肝脏切片的结果表明,人造纳米“血小板”不会在正常组织中产生凝血,保证了其安全性。同时,肿瘤血管标记的荧光切片表明,人造纳米“血小板”一方面可以抑制新生血管的生成,另一方面可以阻断已形成的肿瘤血管。从而达到彻底破坏肿瘤血管系统以“饿死”肿瘤的目的。
3. 结论
综上所述,本研究提出了用于肿瘤血管处精准启动凝血的人造纳米“血小板”,一种高效且安全的的肿瘤血管栓塞剂,并且探究了其达到最佳治疗效果的尺寸。人造纳米“血小板”通过静脉注射即可实现有效的靶向栓塞,具有给药方式简单和适用性广泛的特点。人造纳米“血小板”通过内源性凝血可以适应各种大小的血管,产生持久的栓塞以创造强大的肿瘤“饥饿”治疗条件,有望成为一种可临床应用的新型抗肿瘤治疗策略。
暨南大学生物医学工程研究所薛巍研究员、戴箭副研究员为论文的通讯作者,博士生宗晓晴、硕士生刘腊梅为论文第一作者,暨南大学第一临床医院影像科史长征主任医师对本研究提供了技术指导和帮助。本研究得到了国家自然科学基金项目、广东省自然科学基金项目、广州市科技项目和学校项目等支持。
来源 | Materials Views 、 生命科学技术学院公众号